今ある治療方法・医薬品、診断方法は、人に対して、“効果があることが期待される治療方法や医薬品” 、“病気の診断ができると期待される診断方法”を見つけ出し、人に対して試験を行い、証明してきました。効果の証明は、下記のような方法で行います。
- いまの治療方法と新しい治療方法との効果を比較する
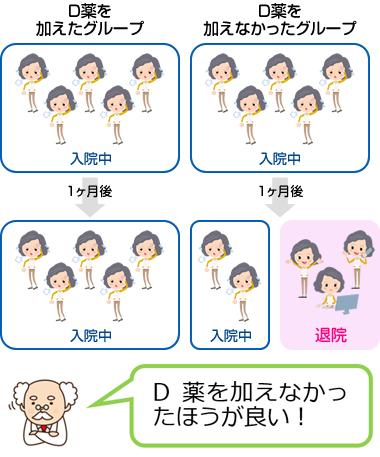
- いまの治療方法のままの群と他の薬を加えた群を比較する
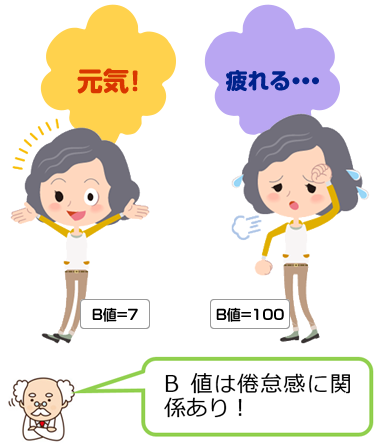
- 検査結果の目標値をグループ別に設定し、どの目標値のグループの健康状態が一番良かったかを比べる
- 同じ病気を持った群の検査結果の傾向を検索する など
現在、たくさんの治療方法や医薬品が存在するのも、人に対して、いろいろな試験が行われ、効果が証明され、確立されてきたからなのです。これも、患者さまのご厚意による協力と研究者たちの努力の賜物なのです。患者さまの協力なくしては、よりよい治療方法を確立することが出来ません。もちろん、“効果が期待される方法”が“必ず効果がある”とは限りませんので、今目の前にいる“研究にご協力いただく方の人権”を優先して、これからのよりよい医療の発展のために試験を行います。
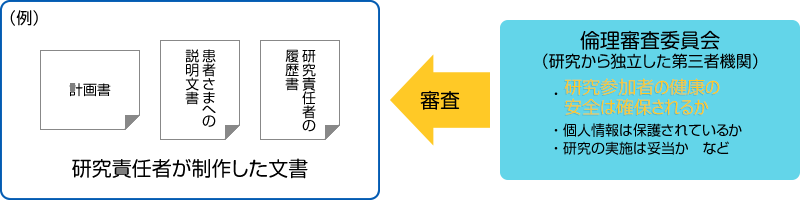
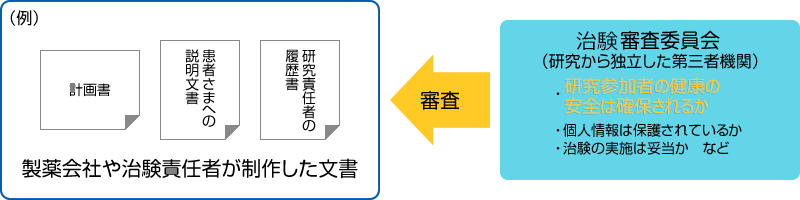
このように、病気の予防・診断・治療方法の改善や病気の原因の解明、患者さんの生活の質の向上を目的として行われる活動のことを臨床研究(人を対象とした医学系研究)といいます。また、新しい医薬品や医療機器の、国からの承認を得るために行われる、人を対象とした試験のことを特に「治験」といいます。人を対象とした医学系研究・治験を行うにあたっては、様々な決まりごとがあります。
治験・臨床試験・臨床研究の違い
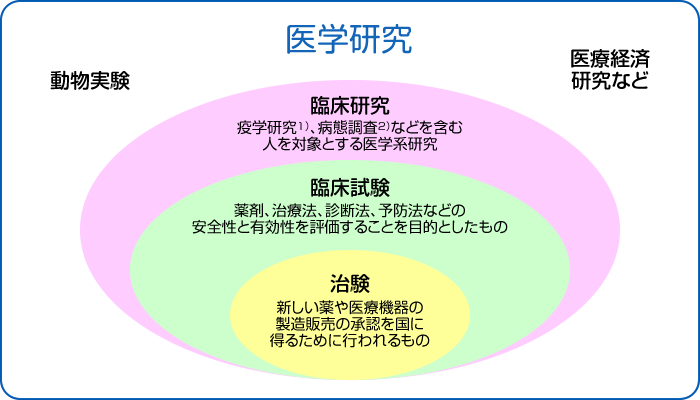
- 1)疫学研究:病気や健康に関する事象の頻度や分布を調査し、その要因を明らかにする科学研究
- 2)病態調査:病気の背景や原因を調査し、病気の成り立ちを明らかにする調査研究
厚生労働省ホームページ 「治験について(一般の方へ)」を参照しました(http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/fukyu.html)